El pH es uno de los conceptos más fundamentales en química y biología, y al mismo tiempo uno de los más utilizados en el laboratorio. Desde el análisis de agua hasta estudios clínicos y procesos industriales, medir el pH permite comprender el comportamiento de las sustancias y su impacto en diferentes sistemas.
Aunque suele representarse con una simple escala numérica, el pH refleja procesos químicos complejos que influyen directamente en reacciones, estabilidad de compuestos y funcionamiento de organismos vivos.
En esta guía completa aprenderás qué es el pH, cómo se mide en laboratorio, qué métodos existen y cuáles son sus principales aplicaciones.
¿Qué es el pH?
El pH es una medida que indica el grado de acidez o alcalinidad de una solución.
Se basa en la concentración de iones hidrógeno (H⁺) presentes en una sustancia.
Cuanto mayor es la concentración de H⁺, más ácida es la solución.
Escala de pH
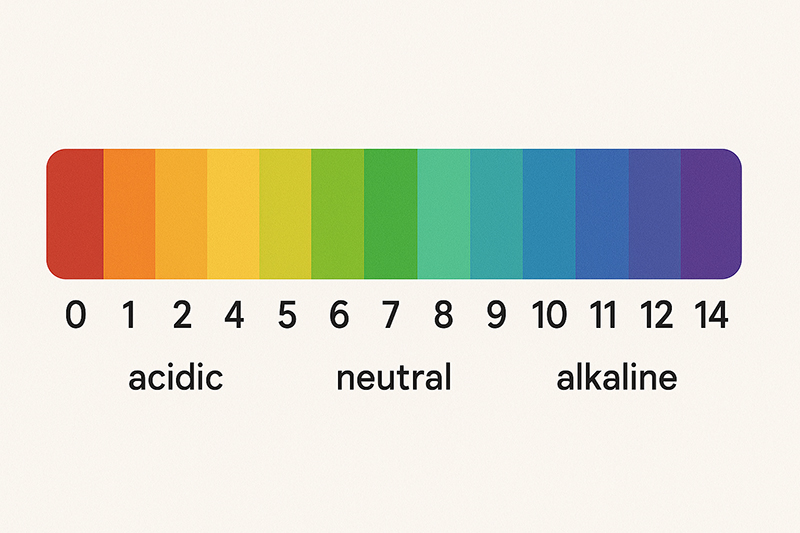
El pH se representa en una escala que va de 0 a 14.
- pH < 7 → ácido
- pH = 7 → neutro
- pH > 7 → básico o alcalino
Ejemplos:
- Jugo de limón → ácido
- Agua pura → neutra
- Solución de jabón → básica
Fórmula del pH
El pH se calcula a partir de la concentración de iones hidrógeno:
pH=−log[H+]pH = -\log[H^+]
Esta relación explica por qué pequeños cambios en concentración generan grandes variaciones en pH.
Importancia del pH en el laboratorio
Medir el pH es fundamental porque influye en:
- Velocidad de reacciones químicas
- Solubilidad de sustancias
- Actividad enzimática
- Estabilidad de compuestos
- Procesos biológicos
Un cambio en el pH puede alterar completamente un experimento.
Métodos para medir el pH en laboratorio
Existen diferentes formas de medir el pH, cada una con su nivel de precisión.
1. Papel indicador de pH
Es uno de los métodos más simples.
Funcionamiento:
- Se introduce el papel en la solución
- Cambia de color según el pH
- Se compara con una escala de referencia
Ventajas:
- Rápido
- Económico
Limitaciones:
- Menor precisión
2. Indicadores químicos
Son sustancias que cambian de color según el pH.
Ejemplo:
- Fenolftaleína
Se utilizan en titulaciones y análisis químicos.
3. pH-metro
Es el método más preciso y utilizado en laboratorio.
Funcionamiento:
- Utiliza un electrodo para medir el potencial eléctrico
- Convierte ese valor en pH
Ventajas:
- Alta precisión
- Resultados rápidos
Es indispensable en análisis profesionales.
Cómo medir el pH correctamente (paso a paso)
1. Preparar el equipo
- Encender el pH-metro
- Verificar calibración
2. Calibrar el pH-metro
Utilizar soluciones buffer (pH conocido).
Este paso es esencial para obtener resultados confiables.
3. Preparar la muestra
- Evitar contaminación
- Homogeneizar la solución
4. Realizar la medición
- Introducir el electrodo
- Esperar estabilización
- Registrar el valor
5. Limpiar el electrodo
- Enjuagar con agua destilada
- Secar correctamente
Mantiene la precisión del equipo.
Errores comunes al medir el pH
No calibrar el equipo
Genera lecturas incorrectas.
Contaminar la muestra
Afecta el resultado.
No limpiar el electrodo
Puede alterar mediciones futuras.
Medir a temperatura incorrecta
El pH depende de la temperatura.
Interpretar mal los resultados
El pH debe analizarse en contexto.
Aplicaciones del pH en química
En química, el pH se utiliza para:
- Controlar reacciones químicas
- Preparar soluciones
- Realizar titulaciones
- Analizar sustancias
Es clave en prácticamente todos los procesos químicos.
Aplicaciones del pH en biología
En biología, el pH es fundamental para:
- Función enzimática
- Procesos celulares
- Equilibrio fisiológico
Ejemplo:
El pH de la sangre humana es ligeramente alcalino (~7.4).
Aplicaciones en la vida real
El pH tiene impacto directo en:
- Calidad del agua
- Industria alimentaria
- Cosméticos
- Agricultura
Controlar el pH es esencial en múltiples industrias.
Relación entre pH y seguridad en laboratorio
Trabajar con sustancias ácidas o básicas requiere precaución.
Riesgos:
- Corrosión
- Reacciones peligrosas
- Daños a la piel
Siempre usar equipo de protección.
Buenas prácticas al trabajar con pH
- Calibrar equipos regularmente
- Usar soluciones buffer confiables
- Mantener limpieza del material
- Registrar resultados
- Controlar condiciones ambientales
El pH es una herramienta esencial para comprender el comportamiento químico y biológico de las sustancias. Aunque su medición puede parecer sencilla, requiere precisión, técnica y conocimiento para obtener resultados confiables.
Desde el uso de papel indicador hasta equipos avanzados como el pH-metro, cada método tiene su lugar en el laboratorio. Lo importante es elegir el adecuado y aplicarlo correctamente.
En el mundo científico, medir el pH no es solo obtener un número: es interpretar cómo una sustancia interactúa con su entorno.